
你是否也曾在深夜清醒地数羊,为失眠所苦?数据显示,我国高达15% 的成年人正与你同病相怜。当安眠药带来依赖风险,认知行为疗法又难以坚持,我们还能怎么办?
近日,发表于国际知名期刊 《Nature and Science of Sleep》 的一项研究,为我们带来了一个令人振奋的答案:经皮耳迷走神经刺激(taVNS)。这种疗法就像在耳朵上贴一个“睡眠贴片”,通过温和刺激便能精准作用于负责放松的神经,从而安全、有效地改善睡眠。它为何能成为非药物疗法的新星?背后的科学原理是什么?让我们一起来了解这个可能改变千万人睡眠的新希望!

一、 失眠的常见病因
慢性失眠是睡眠-觉醒机制失调的表现。睡眠与觉醒脑通路构成一个交互抑制的“翻转开关”,促进两种状态间的快速转换。该过程主要由上行网状激活系统、腹外侧前视前核、中前视前核及下丘脑外侧的促食素能神经元共同调控。上行网状激活系统包括脑干中多种神经元(如胆碱能、单胺能等),并投射至丘脑、前脑基底及皮质,参与维持清醒。
失眠病因复杂,涉及遗传、神经内分泌免疫异常(如HPA轴紊乱)、心理因素及衰老等。其中,过度唤醒被认为是核心机制,即多种因素导致大脑持续处于高度激活状态,影响睡眠-觉醒开关的平衡。Nofzinger等人的PET研究表明,失眠患者大脑代谢水平升高,且与主观睡眠障碍相关。觉醒相关脑区(如上行网状激活系统、下丘脑、丘脑、岛叶、杏仁核和海马体)的功能异常,阻碍了向睡眠状态的转换。此外,失眠患者大脑皮质能量需求更高,易受干扰且唤醒水平升高,进一步支持过度唤醒假说,并解释了夜间睡眠障碍与日间功能下降的现象。
在神经环路层面,一般唤醒系统、情绪调节系统及认知系统共同参与失眠的发生。从功能网络角度看,这些脑区主要属于默认模式网络(DMN)、情感网络(AN)、显著性网络(SN)和中央执行网络(CEN)。功能磁共振成像(fMRI)研究显示,失眠症状与DMN、SN和CEN的连接改变相关。一项英国大型横断面研究进一步表明,频繁失眠与DMN-前额顶叶网络内部连接增强、网络间负连接增加,以及SN与DMN节点连接减弱有关。同时,半球内及半球间交互异常也参与过度唤醒、感觉运动及认知过程,造成睡眠质量的损害。
二、 “taVNS”是什么?
为何选择耳部迷走神经?
迷走神经是包含大量传入纤维的主要副交感神经,负责大脑与器官间的双向信息传递。耳廓是迷走神经在体表的唯一分布区,其耳支(ABVN)密集支配耳甲区等区域。(图1)这使得通过刺激耳部即可直接激活迷走神经传入通路。刺激信号首先传入至孤束核(NTS),进而影响脑干(如蓝斑、缝核)、下丘脑及皮层等广泛脑区,调节自主神经与中枢神经功能。此解剖基础构成了“耳迷走神经传入通路(AVAP)”理论,也是耳部迷走神经刺激(taVNS)的应用依据。
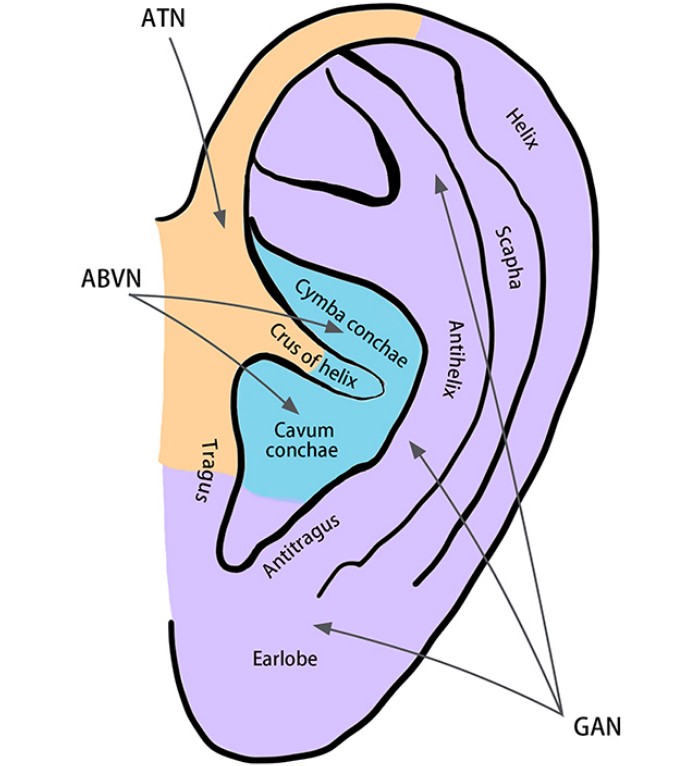
图1 外耳及其可能的神经支配示意图。
在中医理论中,耳甲区等ABVN分布区与调节脏腑功能的耳穴存在重叠。(图2)多项系统评价表明,基于此的耳穴疗法能有效改善睡眠(如延长睡眠时间、提高效率、降低PSQI评分),且比药物不良反应更少。
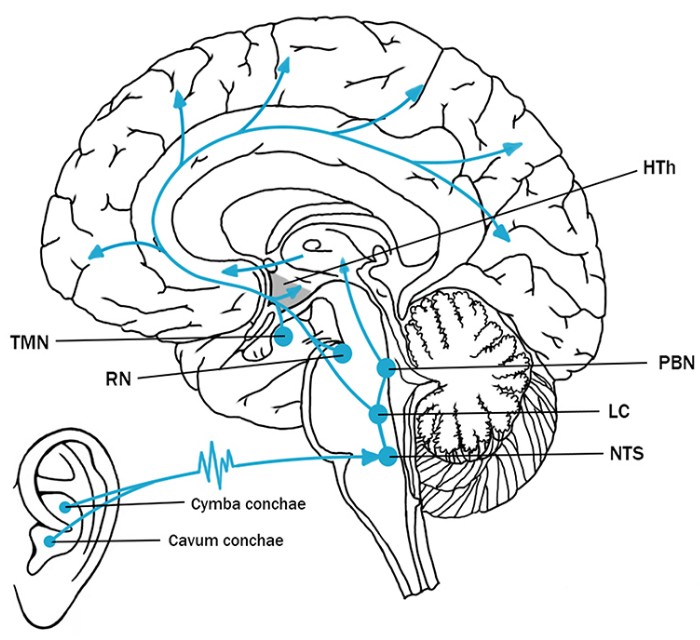
图2 经皮耳部迷走神经刺激可调节与失眠神经病理学相关的脑网络,且ABVN通过NTS投射至多个脑区。
刺激部位与模式
目前,经皮耳迷走神经刺激(taVNS)的最佳靶点与参数尚无统一标准。影像学研究指出,刺激耳屏(尤其是耳甲腔)比刺激耳垂等部位更能有效激活迷走神经核心核团(如孤束核与蓝斑),因此是推荐的刺激部位。
刺激参数需综合考量。频率方面,20Hz或25Hz较为常用,其中25Hz在研究中显示出对心率和大脑活动的显著调节作用,目前针对失眠的研究多采用20Hz。刺激时长则因目标而异,例如每日15分钟持续两周的方案已被证实可改善睡眠与自主神经功能。强度通常由受试者耐受度决定,其安全范围尚待明确。
安全性上,为规避潜在心脏风险(如心动过缓),多数研究倾向于选择左耳进行刺激,但也有研究认为右耳刺激风险未显著增加。该领域仍存在争议,未来需更多高质量研究来确定最佳刺激模式(如单/双侧、左/右侧),并统一对照方法。
三、 taVNS在失眠治疗中的应用
taVNS被认为可通过刺激迷走神经影响脑干核团(如孤束核,NTS),并进一步调节与睡眠、情绪相关的脑区(如皮质和边缘系统)。其作用机制涉及睡眠-觉醒关键通路的调控,例如下丘脑腹外侧视前区(VLPO)通过GABA能神经元抑制觉醒核团(如蓝斑核;中缝背核),促进非快速眼动睡眠(NREM)。这些通路与迷走神经的投射结构存在重叠,因此taVNS可参与睡眠调节。
临床观察显示,taVNS在改善癫痫、抑郁患者睡眠质量的同时,也对原发性失眠具有治疗潜力。多项研究表明,taVNS能降低匹兹堡睡眠质量指数(PSQI)、汉密尔顿抑郁量表(HAMD)及汉密尔顿焦虑量表(HAMA)评分,提升睡眠效率与深睡眠(N3期)比例,缩短入睡潜伏期(SOL)。近期一项为期8周的随机对照试验(RCT)进一步证实taVNS可带来持续疗效。(表1)
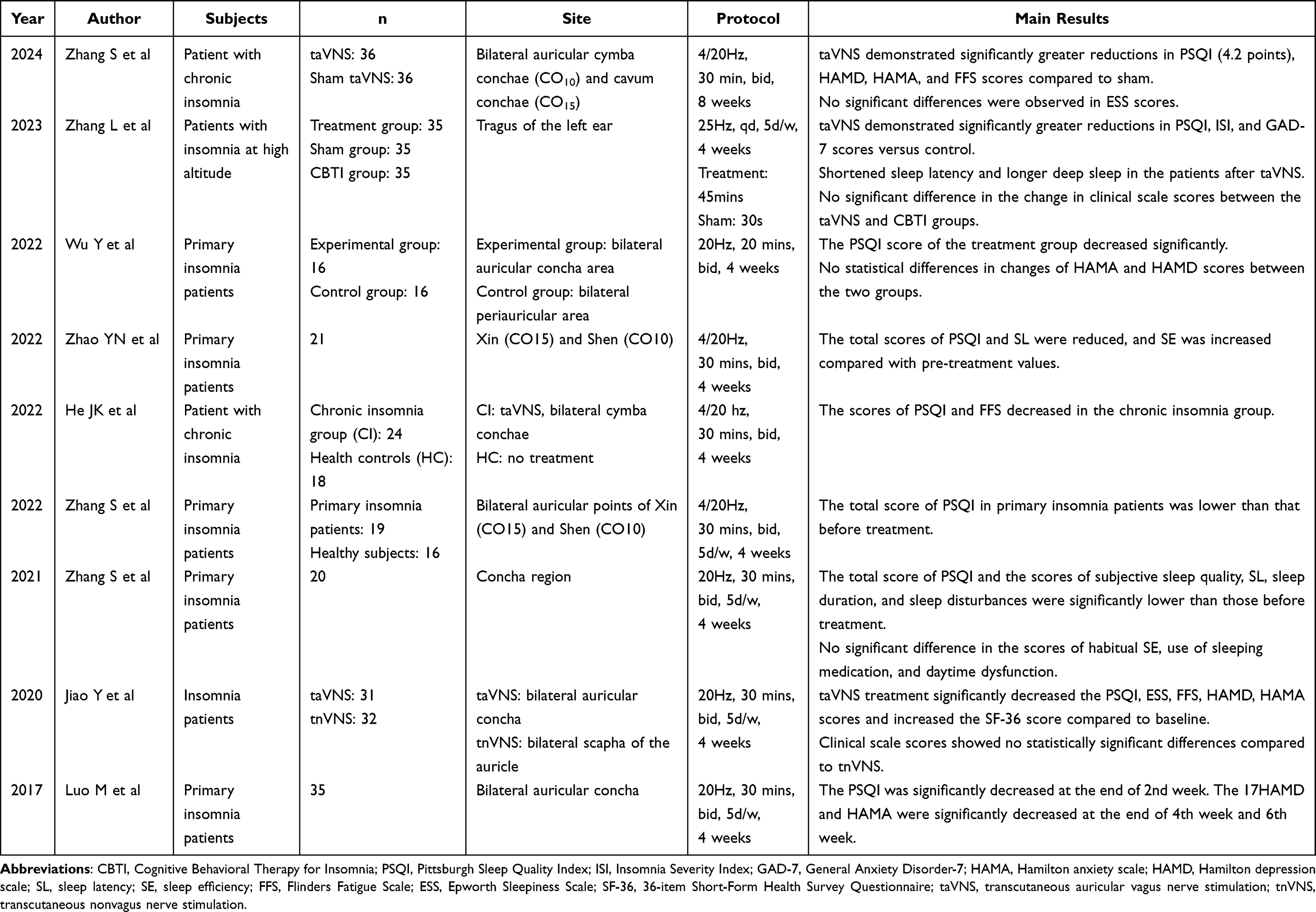
表1 近期完成的经皮耳迷走神经电刺激治疗失眠临床试验
然而,该领域研究仍存在局限:多数样本量小(n<50)、随访时间短(常为4周)、部分研究未设对照,且结果不一,个别研究未显示统计学显著差异。此外,各研究中刺激参数与方案不一致,影响了结果的可比性与证据强度。
四、 taVNS治疗失眠的可能作用机制
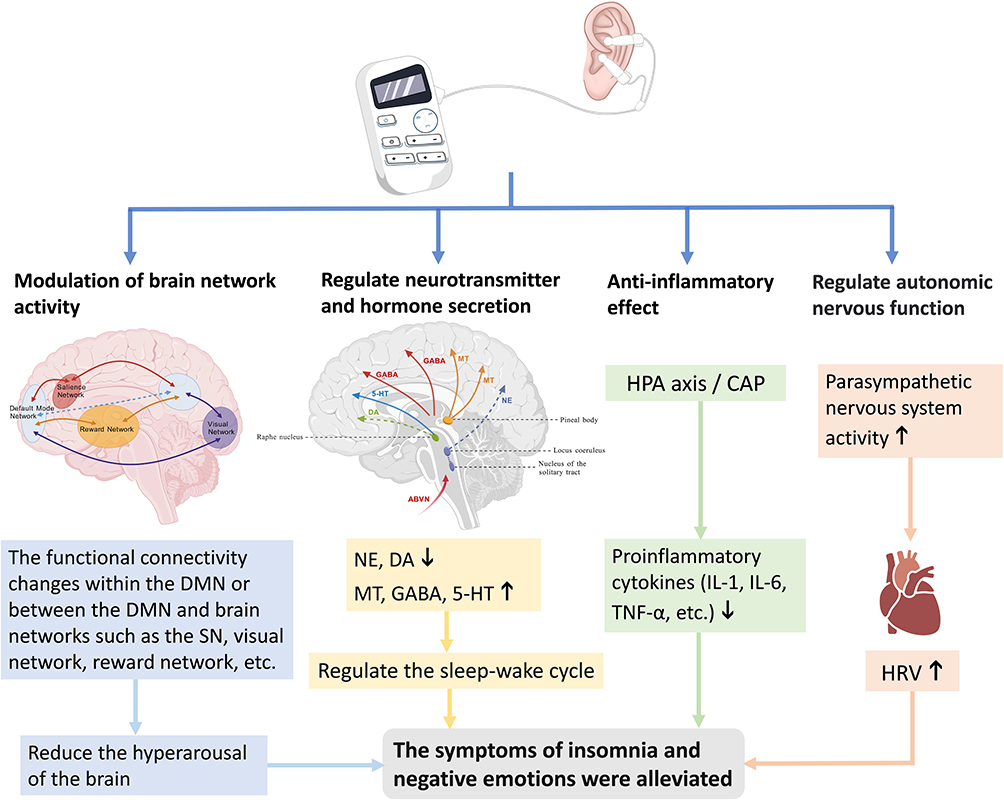
图3 taVNS装置及治疗失眠的四种可能机制。
taVNS治疗失眠涉及多系统调节,其可能机制如下:
调节脑功能网络
神经影像学(如fMRI)发现,taVNS可调节失眠患者过度活跃的脑网络。
默认模式网络(DMN):taVNS可降低DMN内部及其与认知控制网络(CCN) 和突显网络(SN) 之间的异常功能连接,从而降低清醒度,促进睡眠。
丘脑功能:taVNS能改善丘脑与感觉、认知脑区的异常连接,减轻丘脑功能障碍导致的皮质过度兴奋。
影响视觉与感觉处理
taVNS可调节视觉皮层的异常活动,并减弱其与前额叶等脑区的过度连接,从而降低失眠患者对声光刺激的敏感性,缓解入睡前的过度唤醒。
调控情绪与内省
taVNS通过影响与情绪相关的脑区(如杏仁核、前扣带回(ACC))和奖赏回路,减轻伴随失眠的负性情绪。同时,通过调节楔前叶等活动,抑制与失眠相关的内省思维,减少DMN的过度激活。
调节神经递质与激素
褪黑素:taVNS可能通过激活副交感神经,促进褪黑素分泌,调节睡眠-觉醒节律。
γ-氨基丁酸(GABA):taVNS可能提升中枢GABA水平,抑制皮层过度兴奋。
去甲肾上腺素(NE) 与5-羟色胺(5-HT):taVNS可通过孤束核(NTS)-蓝斑核(LC) 通路调节NE系统,并影响5-HT等单胺类神经递质,共同稳定睡眠-觉醒平衡。
抗炎效应
taVNS可能通过激活胆碱能抗炎通路(CAP),抑制白细胞介素(IL-1, IL-6) 和肿瘤坏死因子-α(TNF-α) 等促炎因子的释放,缓解神经炎症,从而改善睡眠。
调节自主神经功能
taVNS通过刺激耳甲区迷走神经,增强副交感神经活性,这通常表现为心率变异性(HRV) 的增加,从而纠正失眠患者的自主神经功能失衡,改善睡眠质量。
五、 未来研究方向
尽管经皮耳迷走神经刺激(taVNS)在失眠治疗中展现出潜力,但其临床应用仍存在多个关键问题有待深入研究。
未来研究应致力于扩大样本量、规范对照组设置与刺激参数、并依据失眠类型进行疗效分层,以确立最佳治疗模式。
当前研究多关注taVNS治疗后的效应,尚缺乏对刺激过程中脑功能与自主神经状态动态变化的深入探究,亦未明确疗效与自主神经指标(如心率变异性HRV)的相关性,导致其脑机制尚未完全阐明。
此外,个体疗效差异显著,需明确其预测因素与适用人群。鼓励采用多技术手段(如神经影像、脑电图及动物实验)综合探究taVNS对神经-内分泌-免疫网络的整体调控作用。值得注意的是,近期证据提示taVNS联合慢速呼吸等整合疗法可能获得更优且持久的疗效,尤其对重症失眠患者。因此,探索taVNS与其他干预措施的协同效应,亦是未来的重要方向。
六、 结论
我们的综述表明,经皮耳迷走神经刺激(taVNS)可能是一种具有前景的神经调控方法,其操作便捷且安全性高,可帮助减轻失眠症状及严重程度,并改善与失眠相关的负面情绪。
taVNS对人体的影响具有系统性和广泛性。我们推测taVNS通过调节脑网络、神经递质与激素分泌以及自主神经功能来缓解失眠症状,但具体机制尚不明确。目前,部分采用taVNS治疗失眠的研究方案存在缺陷,且多数研究样本量较小,不足以提供高质量的失眠治疗证据。此外,关于疗效持续时间、最佳刺激部位及参数设置尚未达成共识。因此亟需开展设计严谨、规模较大且具有长期随访的大型研究。
文献原文链接:https://pubmed.ncbi.nlm.nih.gov/40535058/